
¿Qué es un ion complejo? Características, tipos y ejemplos YuBrain
En química un complejo metálico es una estructura molecular en la que un átomo o ion metálico, generalmente un catión, está rodeado por cierto número de aniones o moléculas dotadas de pares solitarios. Los complejos se llaman también compuestos de coordinación o complejos metálicos y usualmente incluyen al menos un metal de transición.

Forma Geometrica De Orbitales S P D F Simptome Blog

3 Compuestos de Coordinacion. Parte 1 (1) Complejo de Coordinación Quelación Prueba
Los compuestos de coordinación presentan una serie de propiedades físicas y químicas únicas, debido a la presencia de un ion metálico central y los ligandos que lo rodean. En cuanto a las propiedades físicas, los compuestos de coordinación suelen ser sólidos cristalinos, con puntos de fusión y ebullición elevados.
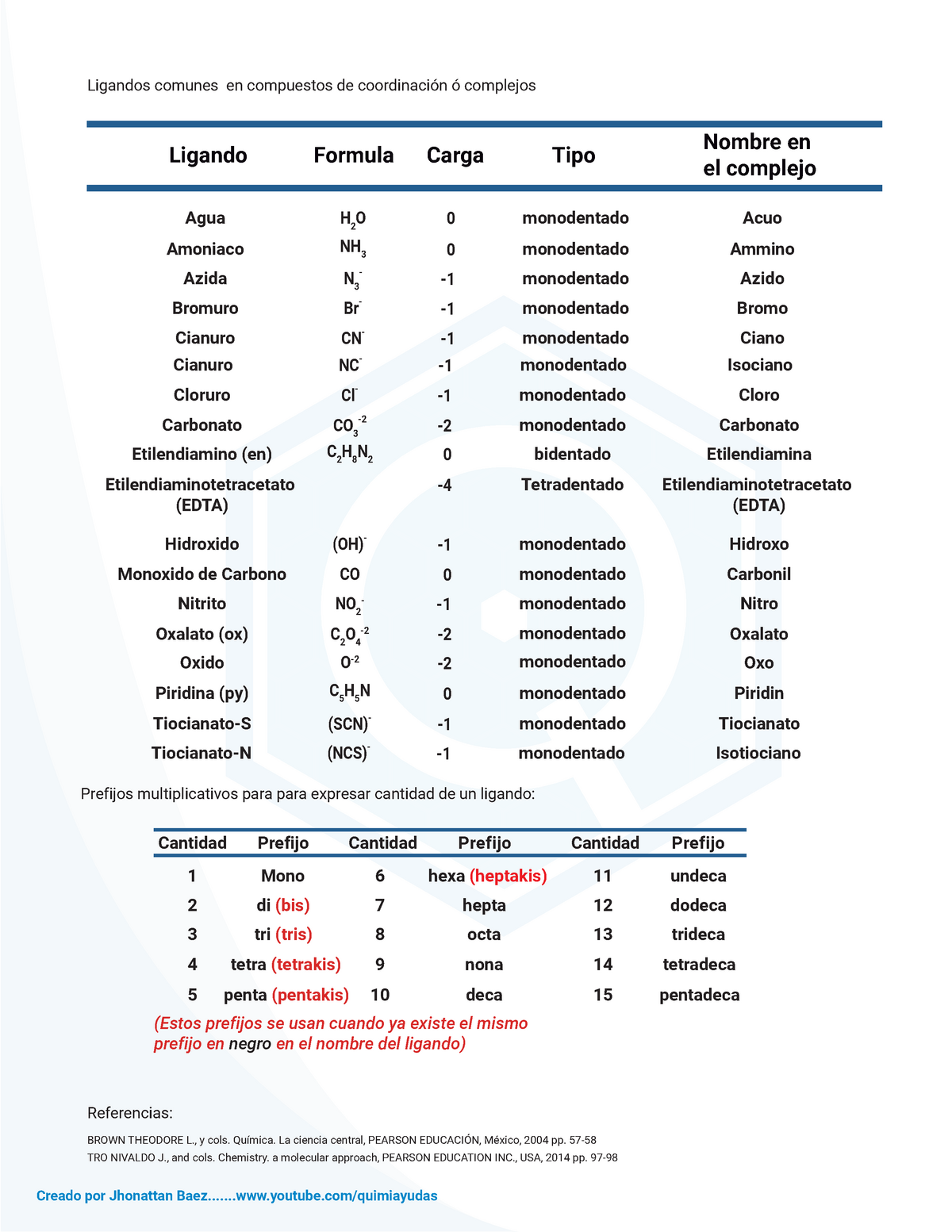
Tabla ligandos complejos, iones comunes Creado por Jhonattan youtube/quimiayudas Ligando
Los átomos o iones centrales y los átomos donantes constituyen la primera esfera de coordinación. La coordinación se refiere a los "enlaces covalentes coordinados" (enlaces dipolares) entre los ligandos y el átomo central. Originalmente, un complejo implicaba una asociación reversible de moléculas, átomos o iones a través de enlaces.

justifica la formacion de los iones a partir de la estructura electronica del atomo neutro
Es la teoría más poderosa, pero también la más complicada. Básicamente, es la teoría orbital molecular aplicada a compuestos de coordinación. Puede hacer declaraciones detalladas sobre el número de enlaces y formas de moléculas, y puede explicar el magnetismo y las propiedades ópticas de los compuestos de coordinación.

¿Qué diferencia los compuestos iónicos y los covalentes o moleculares? Curiosoando
COMIDA PARA LLEVAR CLAVE. Los compuestos de coordinación son una característica importante de la química de más de la mitad de los elementos. Los compuestos de coordinación tienen un papel importante como catalizadores industriales en el control de la reactividad y son esenciales en los procesos bioquímicos.
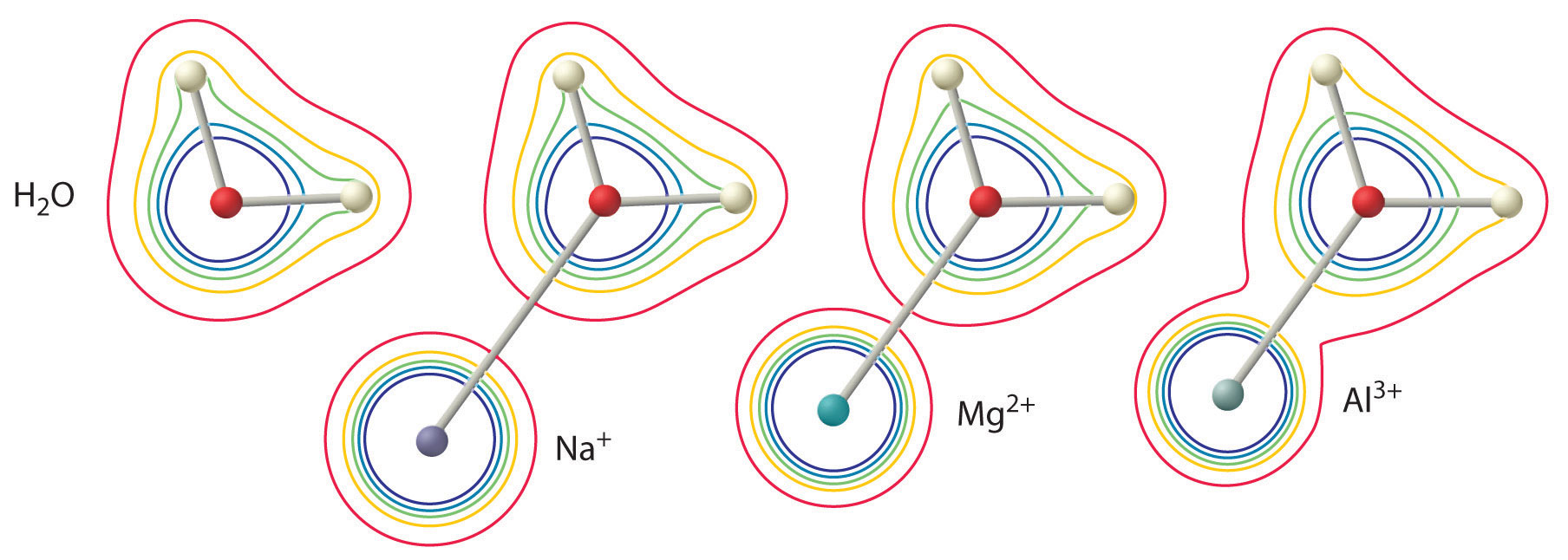
6.3.8 Los iones metálicos de alta relación cargatamaño actúan como ácidos Brønsted en el agua
Un ion complejo es una especie química formada por un átomo metálico central, muchas veces con estado de oxidación positivo, el cual está enlazado por un grupo de moléculas neutras o iones negativos, por medio de enlaces covalentes dativos o coordinados. Al átomo metálico central se le denomina centro de coordinación (por lo que se.
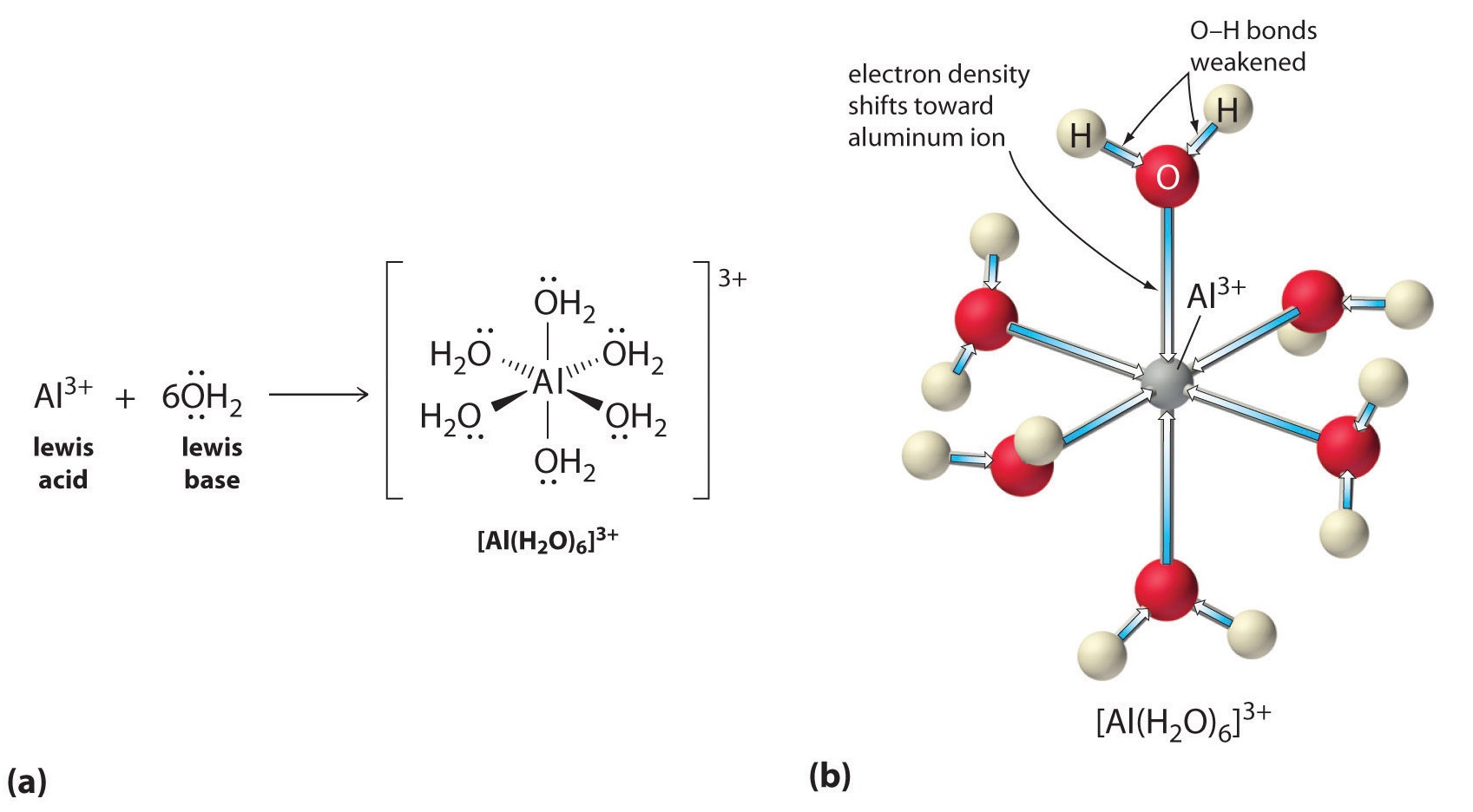
6.3.8 Los iones metálicos de alta relación cargatamaño actúan como ácidos Brønsted en el agua
Figura 14.6.1 14.6. 1: Formación de un complejo ácido-base de Lewis. Un ejemplo de un complejo de coordinación es el dicloruro de hexaaquo cobalto, Co (H 2 O) 6 Cl 2. Este compuesto contiene un ion Co 2+. Este ion metálico electrofílico está coordinado por seis ligandos nucleofílicos de agua.

Cuadro Comparativo De Enlaces Ionicos Covalentes Y Metalicos Xili Porn Sex Picture
CAPITULO UNO COMPLEJOS DE COORDINACIÓN Los elementos metálicos tienden a perder electrones en sus reacciones químicas, lo que da lugar a iones metálicos, sin embargo éstos iones con carga positiva, o cationes,
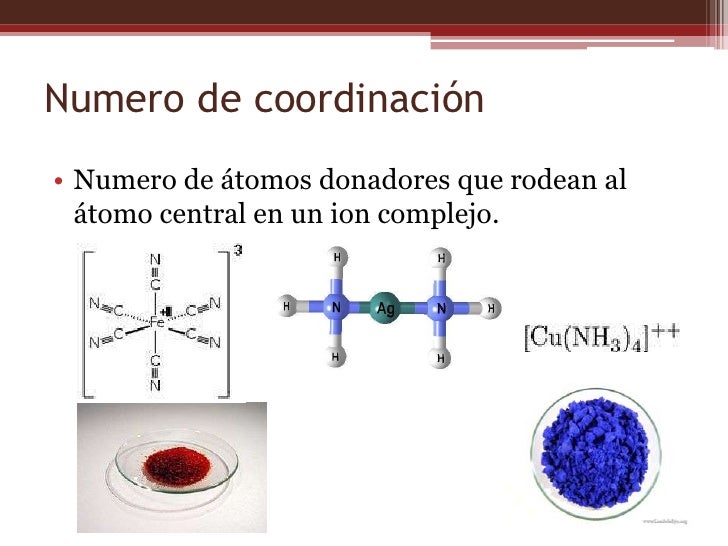
Compuestos de coordinacion
Complejos como el Cu (NH 3) 6 2+ se conocen y estudian desde mediados del siglo XIX. y sus estructuras habían sido elaboradas en su mayoría hacia 1900. Aunque el modelo orbital híbrido pudo explicar cómo las moléculas neutras como el agua o el amoníaco podían unirse a un ion de metal de transición, no pudo explicar muchas de las propiedades especiales de estos complejos.
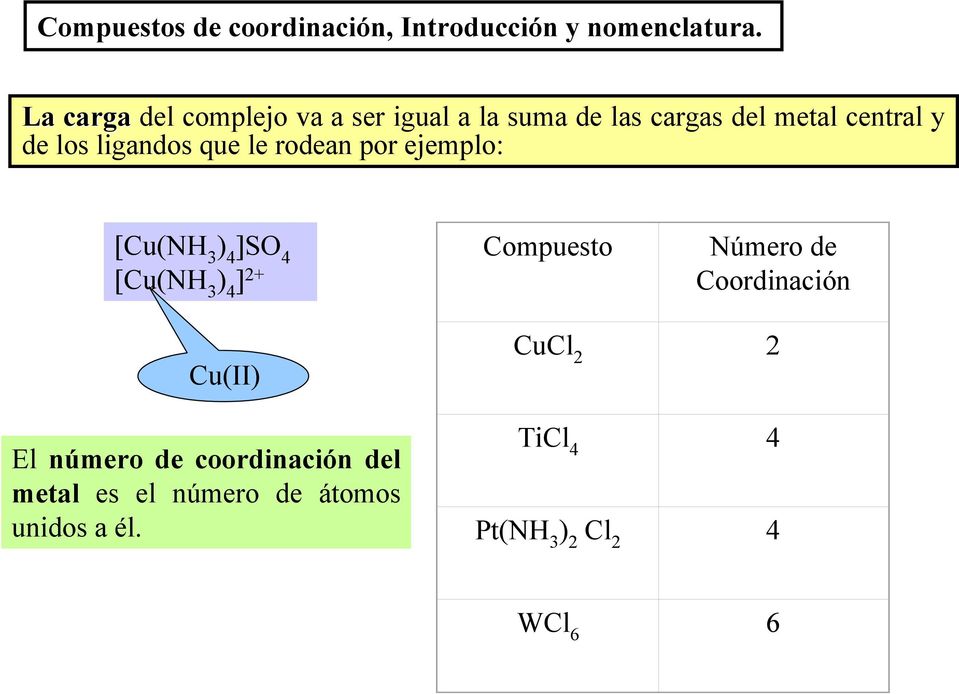
24.3 Nomenclatura de química de coordinación La fisica y quimica
A veces, el nombre latino del metal se usa cuando el nombre en inglés no es adecuado. Por ejemplo, se usa ferrato en lugar de hierro, plomado en lugar de plomo y estannato en lugar de tinado.El estado de oxidación del metal se determina en función de las cargas de cada ligando y la carga total del compuesto de coordinación.

Definición del número de coordinación y ejemplos. YuBrain
Figura 19.12 Los iones metálicos que contienen una subcapa d parcialmente llena forman iones complejos coloreados; los iones con subcapa d (d 0) vacía o con subcapas d (d 10) llenas forman complejos incoloros.Esta figura muestra, de izquierda a derecha, soluciones que contienen iones [M(H 2 O) 6] n+ con M = Sc 3+ (d 0), Cr 3+ (d 3), Co 2+ (d 7), Ni 2+ (d 8), Cu 2+ (d 9) y Zn 2+ (d 10.
Sistemas de coordinación en el ser humano
En química se denomina complejo a una entidad que se encuentra formada por una asociación que involucra a dos o más componentes unidos por un tipo de enlace químico, el enlace de coordinación, que normalmente es un poco más débil que un enlace covalente típico. 1 . Por una costumbre histórica el término complejo se utiliza.
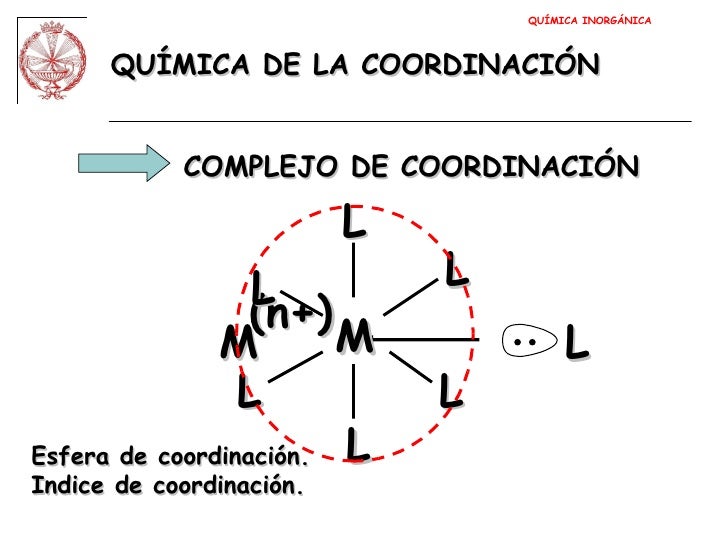
Coordinacion
Responder. Ejercicio 2.13.3 2.13. 3. A menudo, los enlaces múltiples metal-ligando "terminales" podrían estar en equilibrio con ligandos "puente" entre dos átomos metálicos. Mostrar, con dibujos, cómo los ligandos de óxido en dos grupos adyacentes de Fe = O podrían formar una sola unidad Fe 2 O 2. Una segunda clase importante de.
- Cubre Cuello Para Casco Modular
- Efeito Da Cafeina No Organismo
- Rompecabezas Gratis Online De Flores
- Conferencia Intergubernamental Sobre Educación Ambiental 1977
- Mercedes 190 2 5 Turbo Diesel
- Oracion Ala Santa Muerte Para Que Regrese
- Base Cilindro Suda Aceite Low Rider S
- Body Kits For Lexus Is250
- Attention To Diversity Lomce Revised 2016
- Ciudad Del Vino Burdeos Arquitecto